HOME
>
試薬
>
遺伝子工学
>
RNA研究用商品
>
in vivo-jetRNA®+
HOME
>
試薬
>
遺伝子工学
>
トランスフェクション
>
核酸の導入
>
in vivo-jetRNA®+
in vivo専用のmRNAトランスフェクション試薬 in vivo-jetRNA®+
掲載日情報:2022/11/25 現在Webページ番号:65887

追加しました。
- in vivoでのmRNA導入について
- カチオン性脂質を用いたRNA医薬の導入とその問題点について
- 特長
- 操作方法概略
- 使用例
- キット内容
- メーカーポスター
- in vivo-jetRNA®(旧製品)との違いについて
- 価格
in vivoでのmRNA導入について
個体へのmRNA導入は、核酸医薬において有望な手法として期待されています。mRNAの導入は、DNA導入に対する利点として❶高発現(核移行が不要)、❷ゲノムへのインテグレーションが無い、❸免疫への応答性が高いこと(mRNAが自己アジュバント活性を持つことと、十分な免疫反応に必要な抗原量が少なくて済むこと)が挙げられます。また、ウイルスを使用しないため、免疫療法や悪性細胞(malignant cells)を直接標的とする抗がん研究にも効果的な手法です。
追加しました。
カチオン性脂質を用いたRNA医薬の導入とその問題点について
イオン性脂質ナノ粒子(LNP)はRNA医薬のin vivo導入に広く使用されており、主に肝臓を標的としています(Patisiran, BNTech162b, mRNA-1273など)。現在の課題は、市販の脂質を使用し全身投与されたRNAの生体内分布を適切にコントロールし、標的とする臓器や細胞に効果的に送達することです。LNPに使用される古典的なカチオン性脂質(DOTMAおよびDOTAP)は、毒性を誘発するトリメチルアンモニウム基が含まれています。そのほか、イオン化脂質(DLin-MC3-DMA、SM-102、ALC-0315)は生体内分布と安定性に制限があります。Polyplus社が開発したin vivo jetRNA®+はイミダゾール環構造を有する独自のカオチン性脂質であり、毒性が低減されています。
※ 本製品に含まれている新世代のカオチン性脂質LipidBrick IM21.7cについてはこちらをご参照下さい。
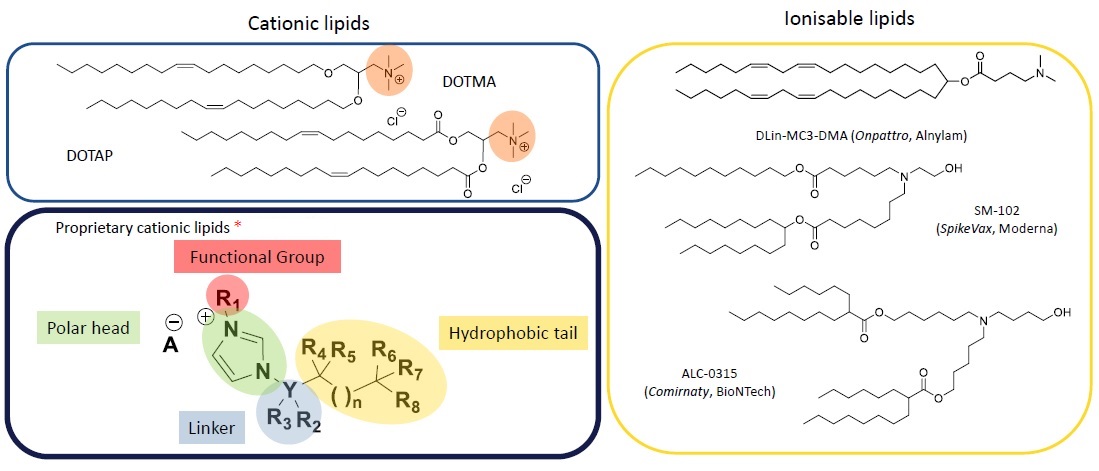
*Basmah N.A., et al., Pharmaceutics, 13(2):206(2021). [PMID:33540942]
追加しました。
特長
- 適応性 :静脈、腹腔内、筋肉内、腫瘍内、皮下など様々なインジェクション方法、標的器官で使用できます。本製品でカプセル化したmRNAを腹腔内投与すると、脾臓やリンパ節のほか、肝臓や肺、膵臓、子宮などにも輸送されます。
- 安全性 :毒性が低く、動物の個体および器官の健康を維持します。
- 時間短縮:インジェクション溶液は2段階で調製することができ、15分で動物に注射する準備が整います。
- アプリケーション例:免疫応答誘発、抗腫瘍研究、CRISPR / Cas9システムを使用したin vivoでのゲノム編集、タンパク製剤の補給
- マウスへの使用回数の目安(in vivo-jetRNA®+ 1 mlあたり):静脈内注射50回、筋肉内注射100回
- 導入分子:mRNA, saRNA, gRNA
追加しました。
操作方法概略
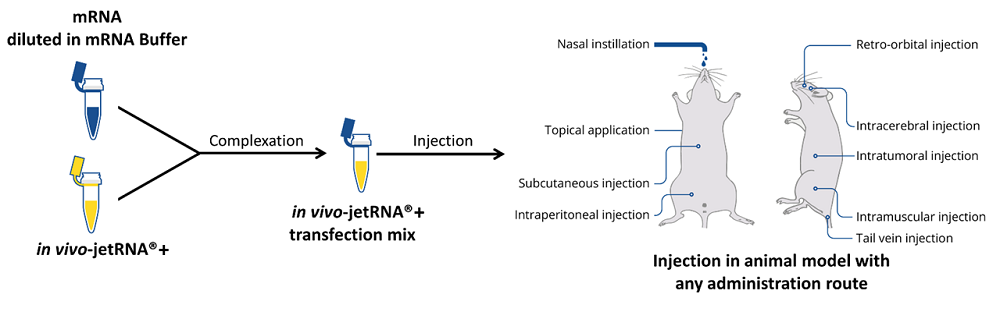
キット付属のmRNA bufferで調製したmRNA(μg)と本試薬(μl)を1:2で混合し、インジェクションするだけのシンプルなプロトコルです。特殊な装置は必要なく、インジェクション用試薬の調製は15分で完了します。
マウスへインジェクションする際の推奨条件
| インジェクション部位 | 出発条件 | 最適化範囲 | インジェクション量 | |
|---|---|---|---|---|
| mRNA | in vivo-jetRNA®+ | |||
| 尾静脈/眼窩後 | 10 μg mRNA 20 μl in vivo-jetRNA®+ |
10~20 μg | 20~40 μl | 200 μl |
| 腹腔内 | 20 μg mRNA 40 μl in vivo-jetRNA®+ |
10~20 μg | 20~40 μl | 500 μl |
| 皮下 | 5 μg mRNA 10 μl in vivo-jetRNA®+ |
5~10 μg | 10~20 μl | 100 μl |
| 皮内 | 2 μg mRNA 4 μl in vivo-jetRNA®+ |
2~5 μg | 4~10 μl | 50 μl |
| 筋肉内 | 5 μg mRNA 10 μl in vivo-jetRNA®+ |
5~10 μg | 10~20 μl | 100 μl |
追加しました。
使用例
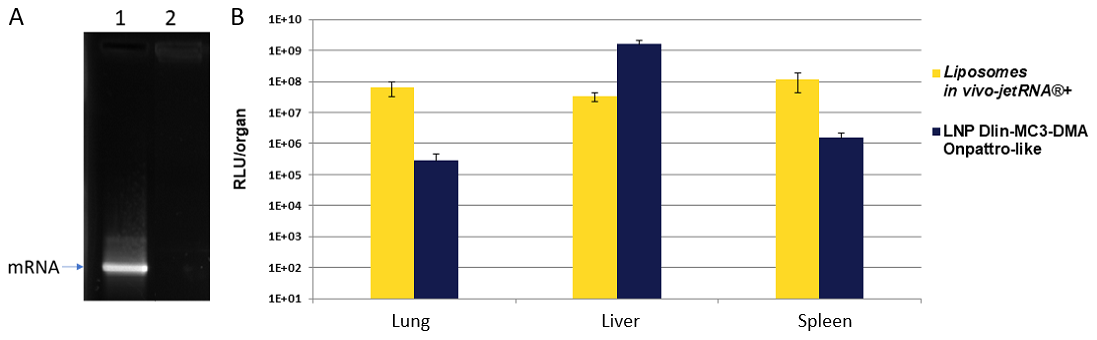
本製品またはDLin-MC3-DMA(LNPを形成)によるmRNAカプセル化の比較
A:mRNAのみ(lane 1)または本製品でカプセル化したmRNA(lane 2)のアガロースゲル電気泳動結果。本製品によりmRNAが完全にカプセル化されていることが分かる。
B:本製品(リポソームを形成)またはDLin-MC3-DMA(pH応答性カチオン性脂質、LNPを形成)を用いて、ルシフェラーゼをコードするmRNAをマウスへ静脈注射した。本製品では10 μgのmRNAを用い、mRNA buffer中でmRNA/本製品の比率が1:2(μg mRNA:μl試薬)となるようにリポソームを形成させた。注射から24時間後にルシフェラーゼの発現を確認したところ、本製品を使用した条件は、ワクチン用のゴールドスタンダードとして使用されているLNPに匹敵する効率で遺伝子発現が観察された。
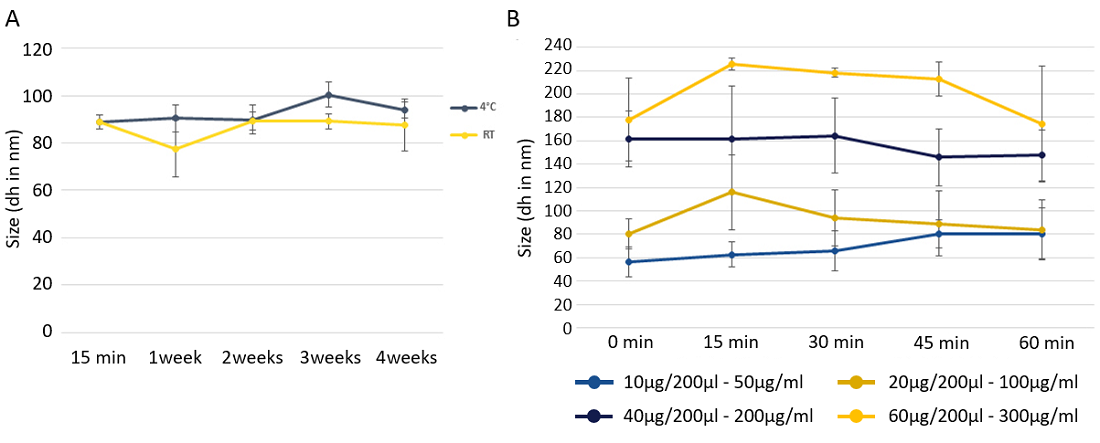
本製品を用いて形成したmRNAカプセル化リポソームの安定性
A:本製品で形成させたmRNAカプセル化リポソーム(50 μg/ml)を、室温または4℃でグラフ中に記載の期間保存後、動的光散乱法(DLS)でリポソームのサイズを測定した。いずれの条件でも、リポソームのサイズは1か月後も安定していることが分かる。
B:本製品と小さいmRNA(1929 base;50、100、200、300 μg)を用いてリポソームを形成させ、グラフ中に記載の時間が経過した後にDLSでリポソームのサイズを測定した。mRNA濃度はリポソームのサイズに影響を及ぼすが、低濃度/高濃度のいずれにおいてもリポソームのサイズが安定していることが分かる。
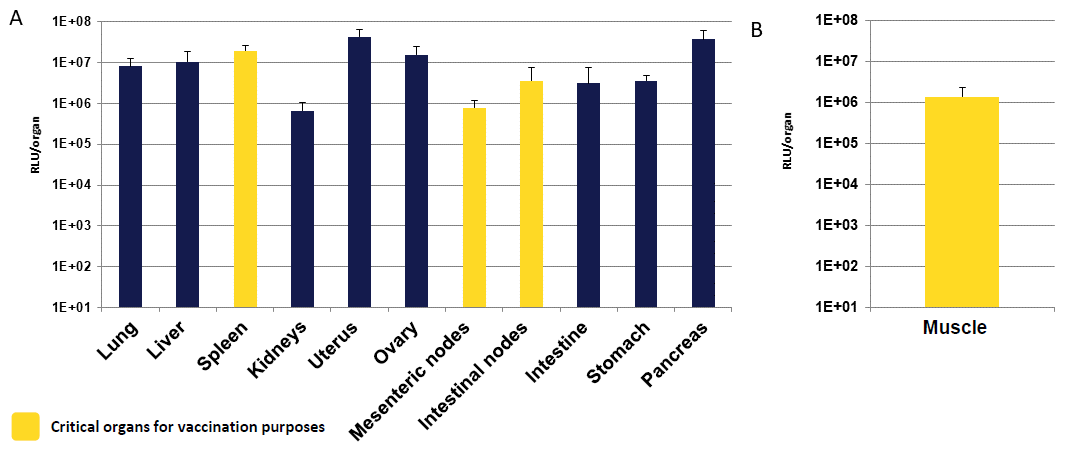
投入経路による各器官におけるmRNAの分布
ルシフェラーゼをコードするmRNA(μg)と本製品(μl)が1:2の比率となるよう混合し、腹腔内(A:20 μg mRNA)または筋肉内(B:5 μg mRNA)へインジェクションした。24時間後に、ルシフェラーゼの発現を測定した。腹腔内投与した場合、免疫応答に関わる脾臓やリンパ節を含め、肺や肝臓、脾臓、子宮など様々な臓器で発現が見られた。
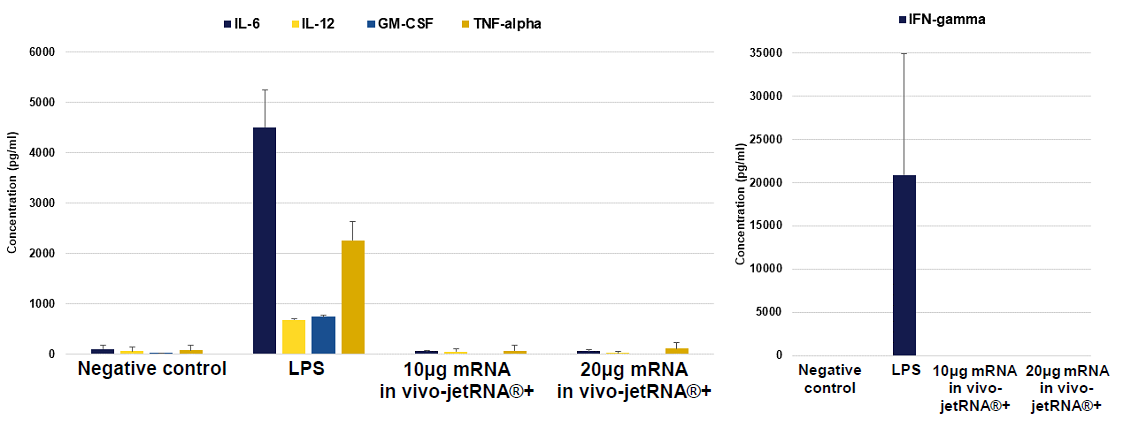
本製品による実験動物への安全性の評価(炎症性サイトカイン量の測定)
ルシフェラーゼをコードするmRNAと本製品を混合してmRNAカプセル化リポソームを形成し、マウスに静脈注射 (眼窩後注射) した。2~24時間後に血液を採取し、IL-6、IL-12、GM-CSF、IFN-γ、TNF-α量をELISA(IL-6)またはMACSPlexキットを用いて測定した。その際にポジティブコントロールとして、LPSを使用した。
本製品を導入した場合、炎症性サイトカインの発現が誘導されていないことが分かる。
追加しました。
キット内容
- in vivo-jetRNA®+ transfection reagent(1 ml)
- mRNA buffer(60 ml)
追加しました。
メーカーポスター

追加しました。
in vivo-jetRNA®(旧製品)との違いについて
in vivo-jetRNA®+(本製品)は旧製品と同じ陽イオン性脂質を含むリポソームベースの試薬になりますが、試薬の組成を改良することで安定性を高めています。本製品は旧製品を用いた場合と比較して、マウスの各臓器に対し同等以上のmRNA導入効率を示すことが確認されています。
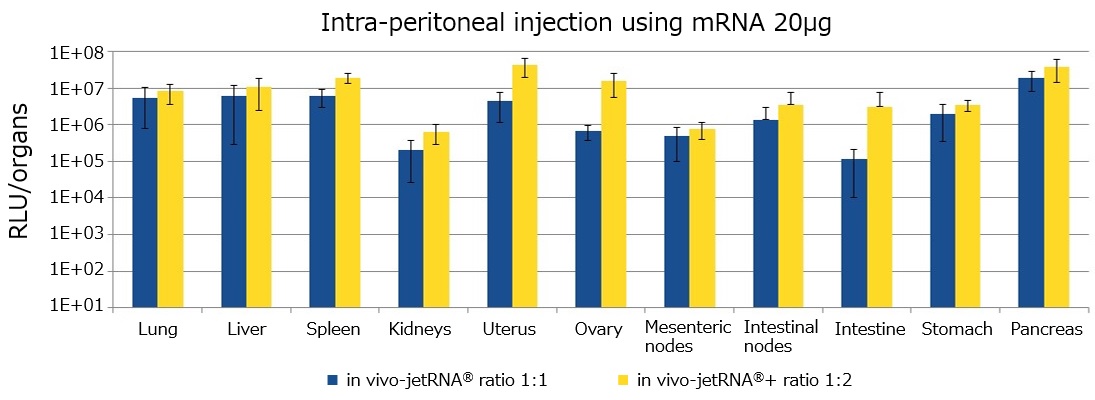
マウスの各臓器に対する本製品および旧製品のmRNA導入効率の比較
本製品および旧製品を用いて、ルシフェラーゼをコードするmRNAを腹腔内注射により導入し、導入効率を比較した。mRNA(ug)と本製品(ul)が1:1(旧製品)または1:2(本製品)になるように混合した。
※1 ugのmRNAあたりの推奨使用量が旧製品よりも増えています。in vivo-jetRNA®+のプロトコルをご参照のうえ、実験条件のご検討をお願いいたします。
追加しました。
価格
[在庫・価格 :2026年06月06日 00時00分現在]
| 詳細 | 商品名 |
|
文献数 | ||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
in vivo-jetRNA+ |
|
0 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
[在庫・価格 :2026年06月06日 00時00分現在]
in vivo-jetRNA+
文献数: 0
- 商品コード:101000122
- メーカー:PPU
- 包装:1kit
- 価格:¥301,000
- 在庫:2個
- 納期:2週間程度 ※※ 表示されている納期は弊社に在庫がなく、取り寄せた場合の目安納期となります。
- 法規制等:
| 説明文 | ※購入時に専用の使用者確認書が必要です。 mRNAの導入に特化したin vivo導入専用のトランスフェクション試薬。毒性が低く,様々なインジェクション方法,標的器官に対応する。シンプルかつ簡単なプロトコルで,15分で試薬が調製できる。 |
||
|---|---|---|---|
| 法規制等 | |||
| 保存条件 | 4℃ | 法規備考 | |
| 掲載カタログ |
ニュース2023年9月15日号 p.19 ニュース2024年3月15日号 p.7 ニュース2024年8月合併号 p.18
|
||
| 製品記事 | |||
| 関連記事 | トランスフェクション試薬選択ガイド mRNAワクチン研究・開発関連製品 トランスフェクション手法の紹介・比較 |
||
追加しました。
おすすめ製品記事
-
Sartorius Polyplus S.A.S.
/ トランスフェクションが困難な細胞へmRNAを導入する試薬
jetMESSENGER® -
Cayman Chemical Company
/ mRNAやsiRNAの送達に適したLipid Nanoparticle(LNP)の作製に関連する製品を取りそろえています!
RNAデリバリーのための脂質ナノ粒子(LNP)作製検討キット・評価用製品 -
Exalpha Biologicals
/ 二本鎖RNA検出用ELISAキット
Double-stranded RNA (dsRNA) ELISA kit -
OZ Biosciences
/ ウイルスフリーでの核酸のドラッグデリバリーシステムに有用な脂質ナノ粒子
NanOZ-LNP Lipid NanoParticlesシリーズ
製品情報は掲載時点のものですが、価格表内の価格については随時最新のものに更新されます。お問い合わせいただくタイミングにより製品情報・価格などは変更されている場合があります。
表示価格に、消費税等は含まれていません。一部価格が予告なく変更される場合がありますので、あらかじめご了承下さい。