HOME
>
試薬
>
タンパク質/酵素
>
タンパク質解析
>
酵素阻害物質スクリーニング/定量キット
>
免疫療法研究用製品(BPS Bioscience社)
HOME
>
試薬
>
タンパク質/酵素
>
タンパク質解析
>
タンパク質間相互作用
>
免疫療法研究用製品(BPS Bioscience社)
HOME
>
試薬
>
免疫化学
>
免疫チェックポイント
>
免疫療法研究用製品(BPS Bioscience社)
がんco-therapyのための初期候補物質探索を支援します 免疫療法研究用製品(BPS Bioscience社)
掲載日情報:2022/05/20 現在Webページ番号:70239
BPS Bioscience社では、腫瘍研究に有用な幅広い免疫チェックポイント関連タンパク質に対応したアッセイキットや、阻害因子スクリーニング用キットを取り扱っています。
追加しました。
- BPS Bioscience社 免疫チェックポイント研究用製品/受託サービスのご案内
- 免疫チェックポイントと免疫療法
- チェックポイント阻害因子の併用(CTLA4およびPD-1)
- PD-1との併用療法のための標的因子としてのLAG3
- Janus Kinase/STAT経路
- PARPとキナーゼの併用
- 多発性骨髄腫の標的因子としてのBCMA
- CAR-TによるBCMA標的化の最適化方法
- 資料 IMMUNOTHERAPY
- 参考文献
BPS Bioscience社 免疫チェックポイント研究用製品/受託サービスのご案内
下表の項目をクリックすると、各製品のラインナップがご覧いただけます。
追加しました。
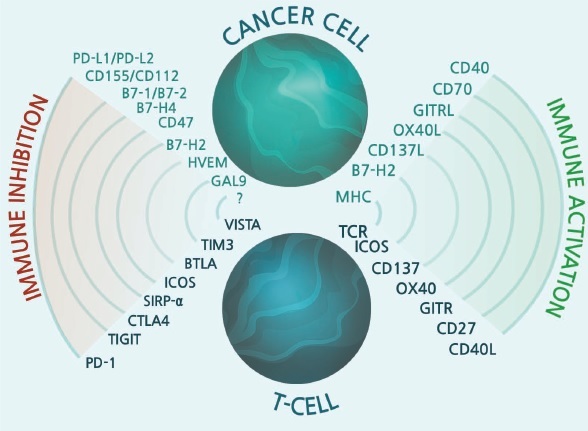
免疫チェックポイントと免疫療法
追加しました。
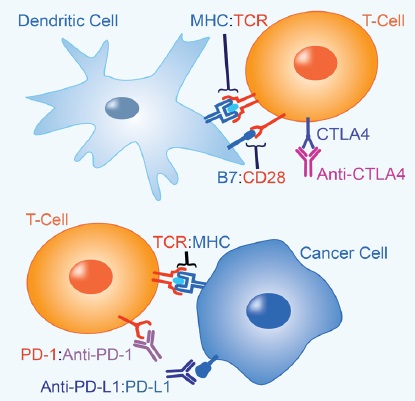
チェックポイント阻害因子の併用(CTLA4およびPD-1)
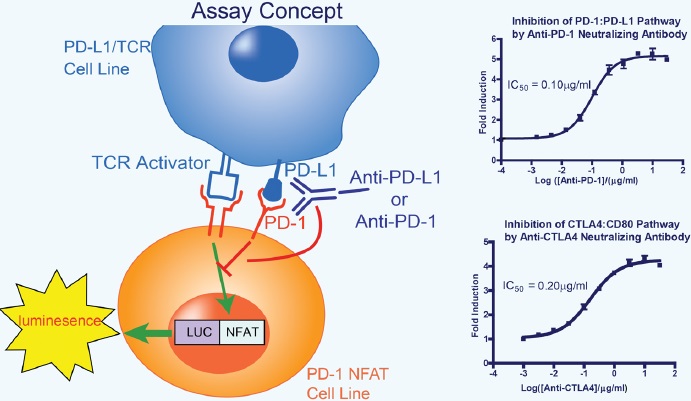
CTLA4およびPD-1免疫チェックポイント経路を標的とする治療用抗体は、現在最も成功している単剤療法です。CTLA4は、最初の臨床的に成功したチェックポイントターゲットであり、B7との相互作用の阻害によってT細胞応答が増加および延長します(右上図)。CTLA4およびPD-1経路を標的化した治療用抗体を組み合わせることで有効性が高まり、転移性黒色腫に対しても有効性が認められています4。
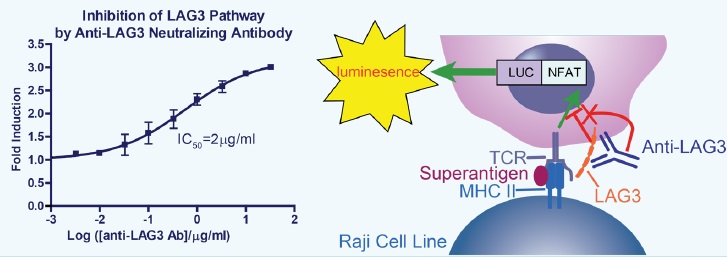
免疫チェックポイントの標的化のための細胞ベースアッセイ
追加しました。
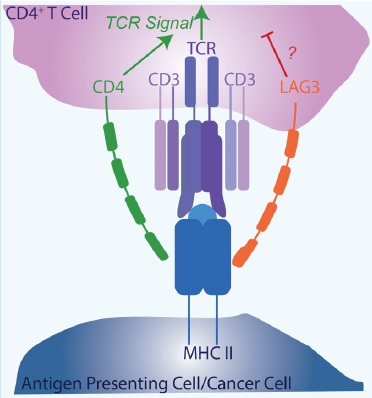
PD-1との併用療法のための標的因子としてのLAG3
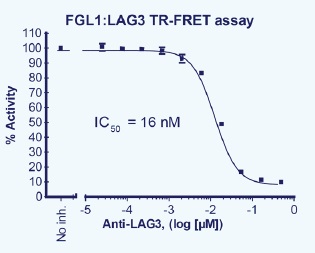
LAG3:FGL1生化学的アッセイ
追加しました。
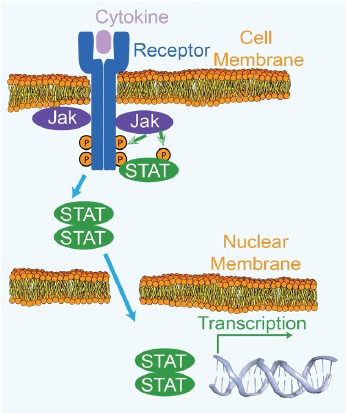
Janus Kinase/STAT経路
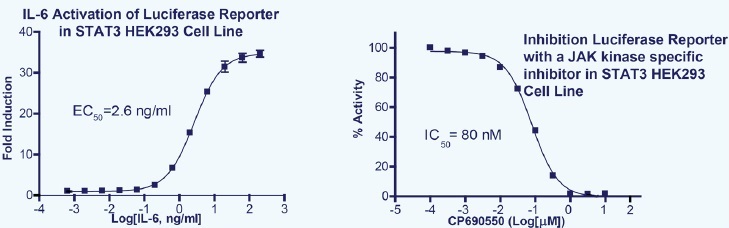
STATレポーターアッセイの検証
JAK2生化学的アッセイ
下図に単離したJAK2キナーゼドメインを用い、JAK2酵素活性を直接標的化した測定例を示した。
JAK2生化学的アッセイの測定例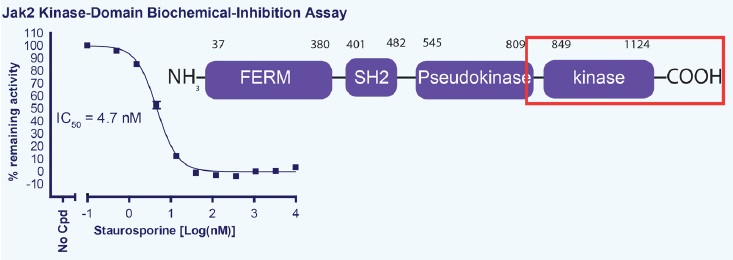
追加しました。
PARPとキナーゼの併用
VEGFR
PARPとVEGFR生化学的アッセイの測定例
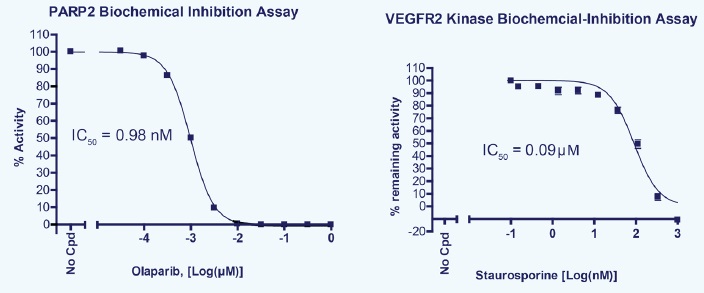
追加しました。
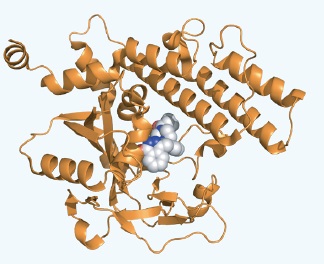
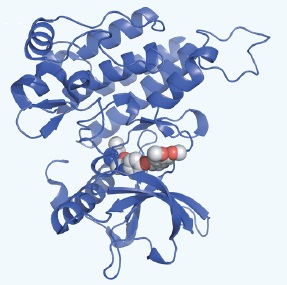
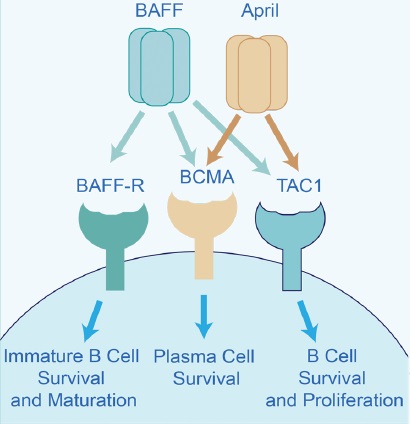
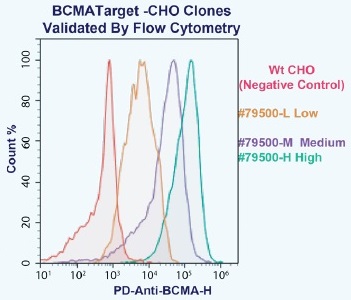
多発性骨髄腫の標的因子としてのBCMA
BCMAに対する生化学的および細胞ベースのアッセイは、CAR構成物とBCMAを基軸としたシグナル伝達の阻害因子のスクリーニングに有用です。
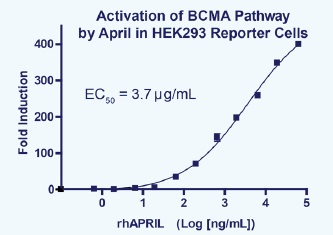
HEK293レポーター細胞を用いたAPRILによるBCMA経路の活性化の測定例
BCMA:リガンドの生化学的アッセイの測定例
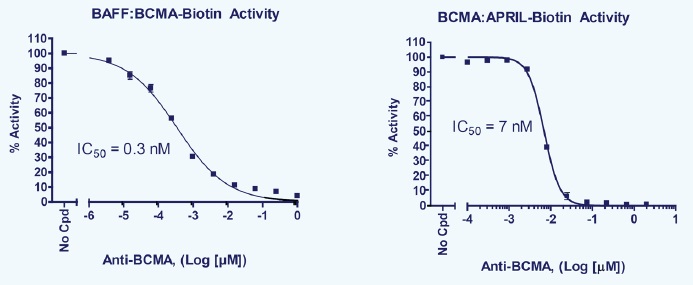
追加しました。
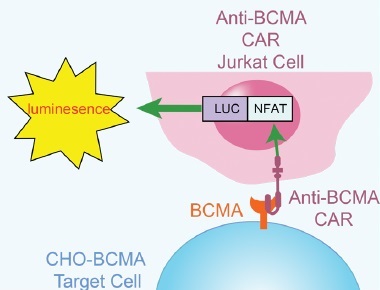
CAR-TによるBCMA標的化の最適化方法
追加しました。
資料 IMMUNOTHERAPY
下の画像をクリックすると、☞ IMMUNOTHERAPY(Brochure)( )をご覧いただけます。
)をご覧いただけます。
追加しました。
参考文献
- Chen, D.S. and Mellman, I., "Oncology meets immunology:the cancer-immunity cycle.", Immunity, 39(1), 1~10 (2013). [PMID:23890059]
- Li, J. et al., "Immune checkpoint receptors in cancer: redundant by design?", Curr. Opin. Immunol., 45, 37~42 (2017). [PMID:28189879]
- Marshall, H.T. and Djamgoz, M.B.A, "Immuno-Oncology: Emerging Targets and Combination Therapies.", Front Oncol., 8, 315 (2018). [PMID:30191140]
- Khair, D.O, et al., "Combining Immune Checkpoint Inhibitors: Established and Emerging Targets and Strategies to Improve Outcomes in Melanoma.", Front Immunol., 10, 453 (2019). [PMID:30941125]
- Andrews, L.P., et al., "LAG3 (CD223) as a cancer immunotherapy target.", Immunol. Rev., 276(1), 80~96 (2017). [PMID:28258692]
- Baumeister, S.H., et al., "Coinhibitory Pathways in Immunotherapy for Cancer.", Annu. Rev. Immunol., 34, 539~573 (2016). [PMID:26927206]
- Huard, B., et al., "Characterization of the major histocompatibility complex class Ⅱ binding site on LAG-3 protein.", Proc. Natl. Acad. Sci. U.S.A., 94(11), 5744~5749 (1997). [PMID:9159144]
- Wang, J., et al., "Fibrinogen-like Protein 1 Is a Major Immune Inhibitory Ligand of LAG-3.", Cell, 176(1~2), 334~347 (2019). [PMID:30580966]
- Vainchenker, W. and Constantinescu, S.N., "JAK/STAT signaling in hematological malignancies.", Oncogene, 32(21), 2601~2613 (2013). [PMID:22869151]
- Pitroda, S.P., et al., "JAK2 Inhibitor SAR302503 Abrogates PD-L1 Expression and Targets Therapy-Resistant Non-small Cell Lung Cancers.", Mol. Cancer Ther., 17(4), 732~739 (2018). [PMID:29467274]
- Jiao, S., et al., "PARP Inhibitor Upregulates PD-L1 Expression and Enhances Cancer-Associated Immunosuppression.", Clin. Cancer Res., 23(14), 3711~3720 (2017). [PMID:28167507]
- Zimmer, A.S., et al., "A phase I study of the PD-L1 inhibitor, durvalumab, in combination with a PARP inhibitor, olaparib, and a VEGFR1-3 inhibitor, cediranib, in recurrent women's cancers with biomarker analyses.", J. Immunother. Cancer, 7(1), 197 (2019). [PMID:31345267]
- Zarnegar, S., et al., "Novel activating BRAF fusion identifies a recurrent alternative mechanism for ERK activation in pediatric Langerhans cell histiocytosis.", Pediatr. Blood Cancer, 65(1), (2018). [PMID:28748614]
- Mackay, F. and Schneider, P., "TACI, an enigmatic BAFF/APRIL receptor, with new unappreciated biochemical and biological properties.", Cytokine Growth Factor, Rev 19(3~4), 263~276 (2008). [PMID:18514565]
- Wang, H., et al., "Immune checkpoint blockade and CAR-T cell therapy in hematologic malignancies.", J. Hematol Oncol., 12(1), 59 (2019). [PMID:31186046]
追加しました。
製品情報は掲載時点のものですが、価格表内の価格については随時最新のものに更新されます。お問い合わせいただくタイミングにより製品情報・価格などは変更されている場合があります。
表示価格に、消費税等は含まれていません。一部価格が予告なく変更される場合がありますので、あらかじめご了承下さい。