細胞質へ導入するタンパク質トランスフェクション試薬 ProteoCarry®(Protein Transfection Reagent)
掲載日情報:2023/05/30 現在Webページ番号:68023

フナコシ /
フナコシ株式会社
[メーカー略称:FNA]
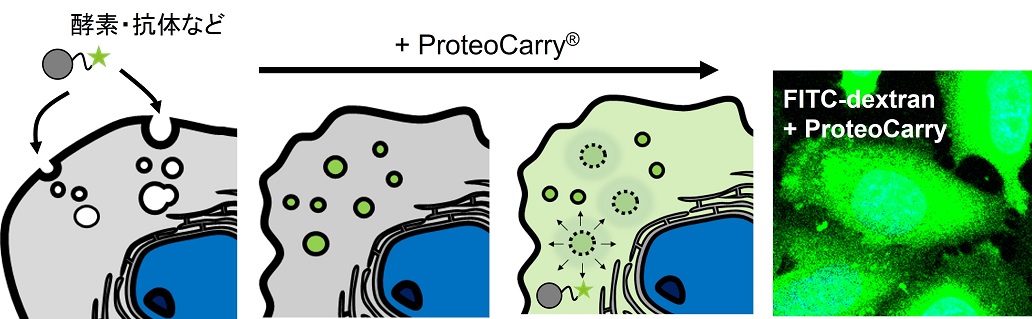
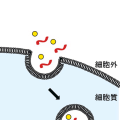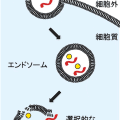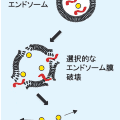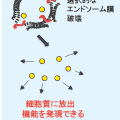
タンパク質およびデキストランなどの生体高分子を細胞内、特に細胞質に導入する試薬です。従来のタンパク質トランスフェクション試薬は導入タンパク質がエンドソーム/リソソームで滞留することが問題視されていましたが、本製品はタンパク質を細胞質に高効率に輸送することができるため、導入タンパク質の細胞内機能の評価や、抗体導入による機能阻害誘導など幅広い実験に使用できます。また従来品と異なり、タンパク質とのプレインキュベーション不要で複合体を形成しないため、タンパク質の機能に与える影響を最小限に留められます。
※ 本製品は研究用です。研究用以外には使用できません。
追加しました。
タンパク質トランスフェクション試薬とその問題点
追加しました。
特長
- ペプチド性のタンパク質トランスフェクション試薬で、高い水溶性を示します。
- 優れたエンドソーム膜破壊活性を示し、従来手法に比べ高い細胞質伝達性を示します。なお、本ぺプチドは☞ エンドソーム膜破壊後もエンドソームに結合したまま留まります。詳細はこちらをご覧下さい。
- 導入物質とのプレインキュベーションが不要で、簡便かつ迅速にトランスフェクション可能です。
- タンパク質と複合体を形成しないため、比較的高濃度のタンパク質を添加する必要がありますが、タンパク質の機能への影響が最小限に抑えられます。
- 1時間の処理で十分に細胞質へのトランスフェクションができます。
- 血清の有無(<10% FBS)による導入効率への影響がありません。使用したい細胞に合わせた実験プロトコルの構築が可能です。
- 様々なタンパク質、生体高分子を細胞質に導入した実績があります。
例:IgG抗体、機能性タンパク質(Cre recombinase, Saporin)、多糖(デキストラン) - 推奨使用濃度では細胞毒性がほとんどありません。
追加しました。
使用方法概略

図をクリックすると拡大します( )
)
- フレッシュな培地(無血清培地、10%以下の含FBS培地またはPBS)に、本製品と導入したいタンパク質などを添加する(以下、トランスフェクション混合液)。
※ プレインキュベーション不要。 - 細胞(80%以下のコンフルエント状態)をPBSで2回洗浄した後、トランスフェクション混合液を細胞に添加する。
- トランスフェクション混合液中で細胞を培養する(1時間~)。
- 細胞をPBSで2回洗浄した後、フレッシュな培地を添加する。
- 各アプリケーションに使用できる。
追加しました。
キット内容
- ProteoCarry®(4 mg)
- FITC-dextran(2 mg、ポジティブコントロール用)
追加しました。
アッセイ回数の目安
| プレートのウェルサイズ | ProteoCarry® | FITC-dextran |
|---|---|---|
| 6 well | 14 assays | 5 assays |
| 12 well | 28 assays | 10 assays |
| 24 well | 56 assays | 20 assays |
| 48 well | 140 assays | 50 assays |
| 96 well | 280 assays | 100 assays |
※ アッセイ回数はデータシートに記載されたプロトコル例を基にした目安です。実験方法・条件によって変動します。
追加しました。
導入実績のある細胞
- HeLa
- SW480
- COS7
- NIH3T3
- HUVEC
追加しました。
導入量の目安
| 導入物 | 培地に対する推奨終濃度 | |
|---|---|---|
| 抗体 | 50~250 μg/ml | |
| タンパク質 | Saporin | 1~10 μg/ml |
| Cre recombinase | 10~100 μg/ml | |
| FITC-dextran (ポジティブコントロール) |
200 μg/ml | |
※ 導入効率は細胞種、細胞数やタンパク質の種類など様々な要因によって変動します。上記は目安であり、実験毎に最適化することをお勧めいたします。
追加しました。
使用例
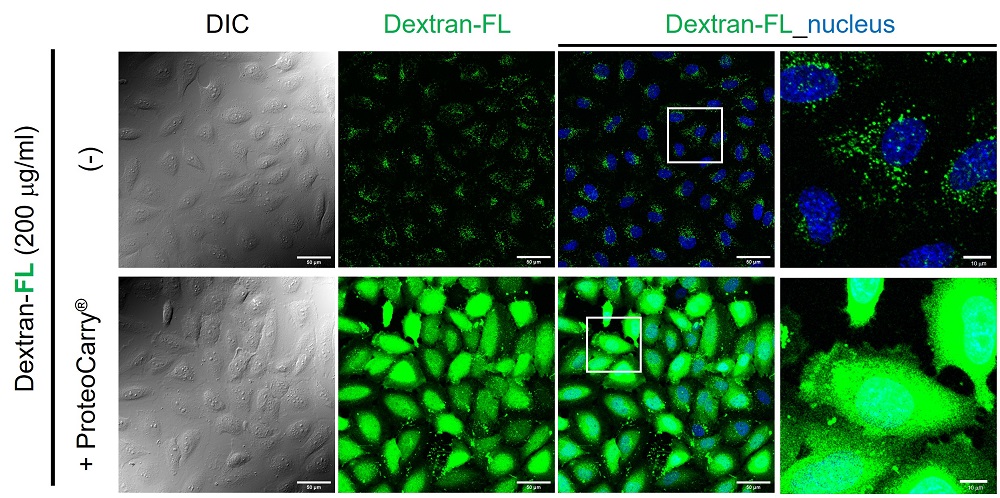
蛍光標識Dextranの導入
HeLa細胞へ蛍光標識Dextran(Dextran-FL;平均分子量10 kDa, 培地に対する終濃度200 μg/ml)を導入した。Dextran-FLのみを細胞に添加した場合(―)はドット状の蛍光シグナルが観察されるものの細胞質ではほとんど蛍光シグナルが観察されなかった。一方、本製品を用いた場合は細胞質全般に蛍光シグナルが観察され、Dextran-FLが細胞質に取り込まれていることが分かる。
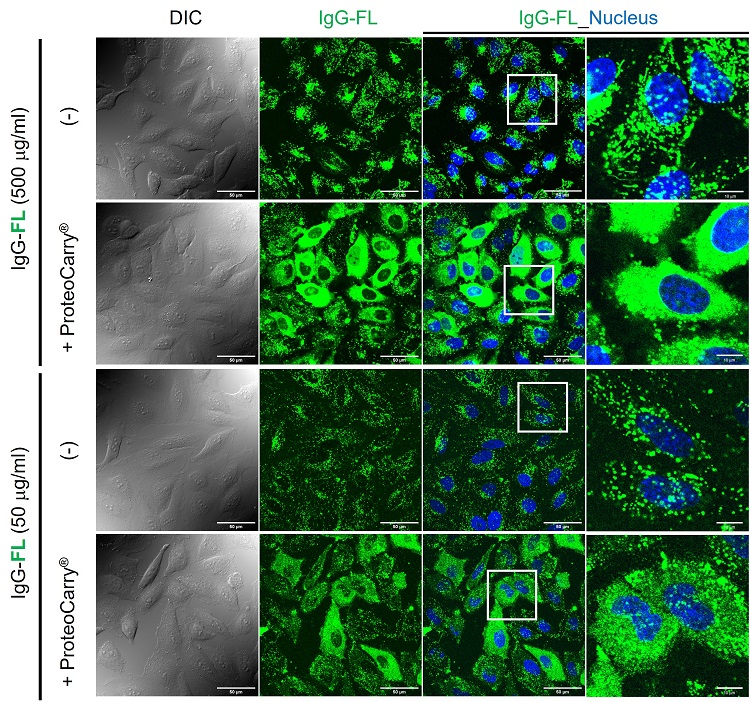
蛍光標識IgGの導入
HeLa細胞へ蛍光標識IgG抗体(IgG-FL、培地に対する終濃度50 or 500 μg/ml)を導入した。IgG-FLのみを細胞に添加した場合(―)、エンドサイトーシスで取り込まれドット状の蛍光シグナルが観察され、エンドソームおよびリソソームに留まっていることが分かる。一方、本製品を用いた場合は、ドット状のエンドソーム構造も観察されるが、細胞質から蛍光シグナルが観察され、エンドソームから細胞内に拡散していることが分かる。
※ 蛍光シグナルで細胞質の拡散を観察する場合、エンドソームに比べ細胞質の体積が大きいためシグナルが希釈されます。導入する蛍光標識因子の量が少ないと、細胞質まで拡散していてもエンドソーム由来の蛍光シグナルが際立って観察される可能性があります。細胞質での蛍光シグナルの検出には、比較的高濃度の蛍光標識タンパク質を添加することを推奨しています。
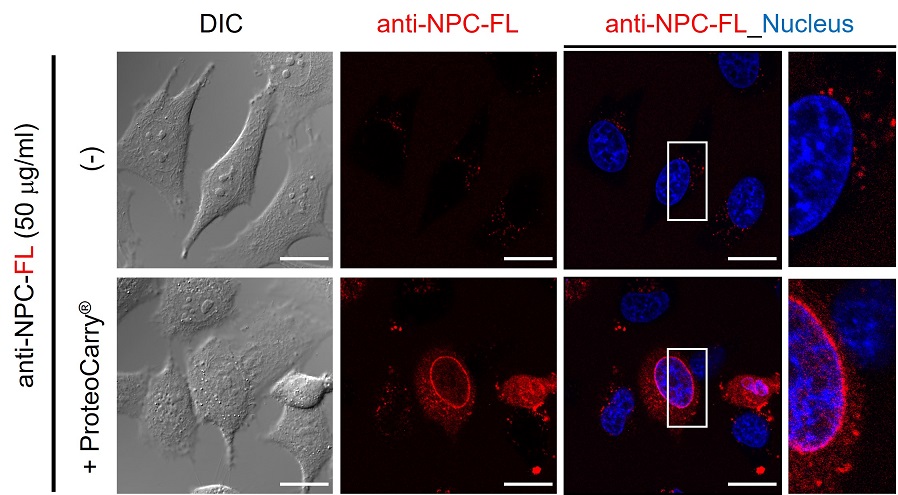
抗核膜孔複合体抗体の導入
HeLa細胞へ蛍光標識した抗核膜孔複合体 (Nucleus pore complex;NPC) 抗体(Anti-NPC-FL;培地に対する終濃度50 μg/ml)を導入した。蛍光標識抗体のみを細胞に添加した場合(―)、ドット状の蛍光シグナルが観察されるのみだが、本製品を用いた場合は、核膜構造が明瞭に観察されており、抗NPC抗体が細胞質に取り込まれたのち核膜構造に結合していることが分かる。
核局在性EGFPの導入
HeLa細胞へ核局在シグナル(NLS)配列を有するEGFP組換えタンパク質(NLS-EGFP、培地に対する終濃度10 μM)を導入した。NLS-EGFPのみを細胞に添加した場合(―)、エンドサイトーシスで自発的に取り込まれドット状の蛍光シグナルが観察され、エンドソームおよびリソソームに留まっていることが分かる。一方、本製品を用いた場合は、ドット状のエンドソーム構造も観察されるが、蛍光シグナルは主に核に局在しており、NLS-EGFPが細胞質に取り込まれたのち核に移行していることが分かる。
Cre recombinaseの導入
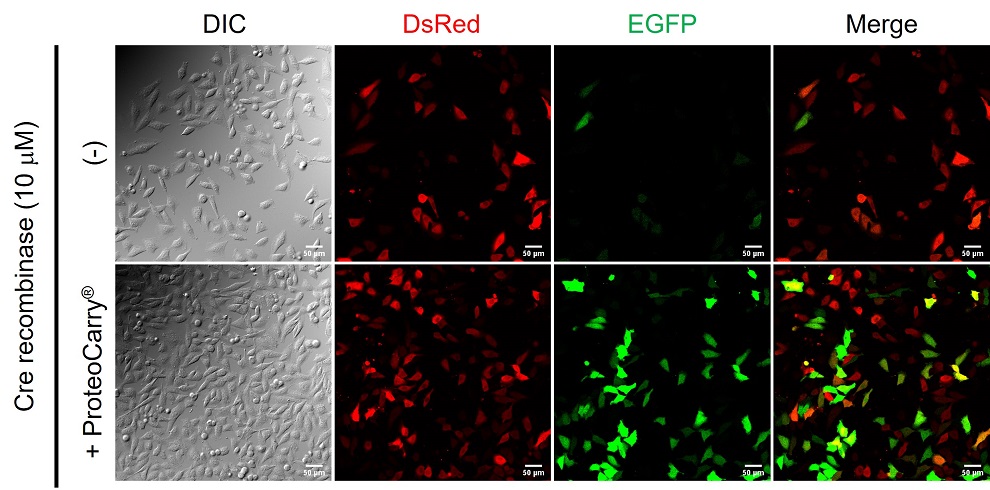
Cre recombinase非存在時にはDsRedが発現し、Cre recombinase存在時にのみ組換えが起こりGFPを発現するようにデザインされたプラスミド(loxP-DsRed-Stop-loxP-EGFP)をHeLa細胞に遺伝子導入した。プラスミド導入翌日にDsRedを発現しているHeLa細胞に対して、本製品を用いてHisタグ融合タンパク質として発現・精製したCre recombinase(培地に対する終濃度10 μM)を導入した。細胞内導入されたCre recombinaseに依存してGFPが発現しており、本製品がCre recombinaseの機能を維持したまま細胞質に導入できることが分かる。
酵素依存的毒素タンパク質Saporinの導入
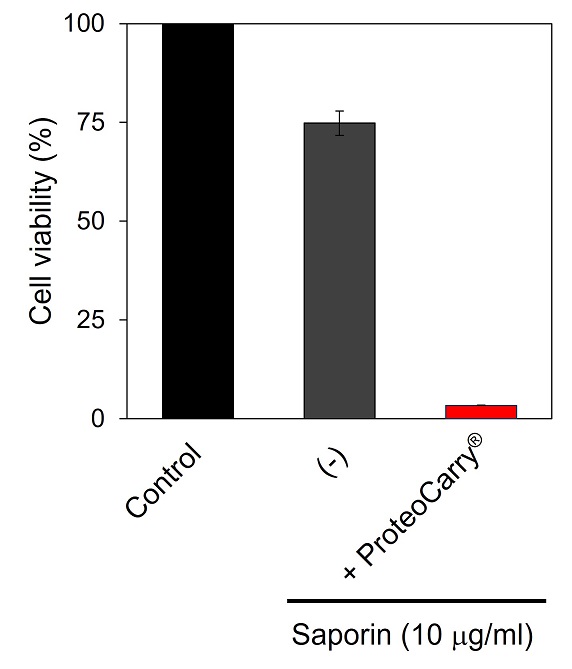
Saporinは植物由来のタンパク質で、リボソームに直接結合しRNAグリコシダーゼ活性によりリボソームを不活性化することで細胞死を誘導する毒素タンパク質である。
RAW264.7細胞へSaporin(培地に対する終濃度10 μg/ml)を導入した。Saporinのみを細胞に添加した場合の細胞生存率は75%程度であったが、本製品を用いた場合は、大部分が死滅していることが分かる。本製品により、Saporinが酵素活性を維持したまま細胞質に輸送され、リボソームに作用していることを示している。
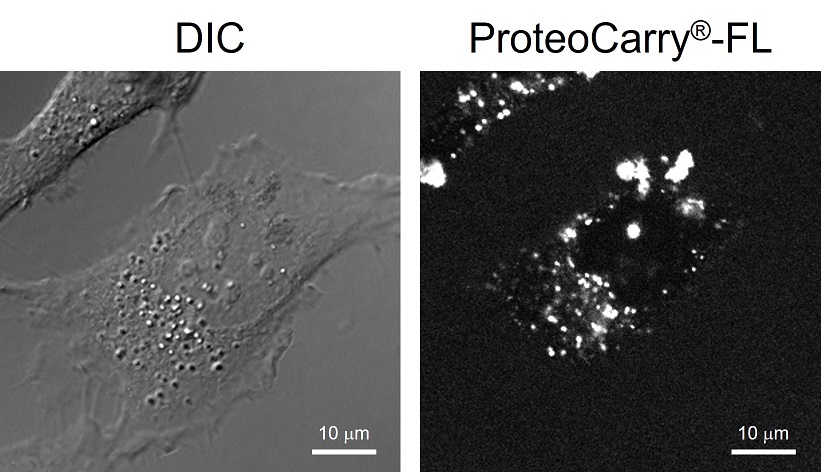
参考データ:ProteoCarry®の細胞内局在
追加しました。
ProteoCarry® ご使用ユーザー様の声
追加しました。
価格
[在庫・価格 :2025年07月19日 08時15分現在]
| 詳細 | 商品名 |
|
文献数 | ||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
ProteoCarry <Protein Transfection Reagent> |
|
0 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
[在庫・価格 :2025年07月19日 08時15分現在]
ProteoCarry <Protein Transfection Reagent>
文献数: 0
- 商品コード:FDV-0015
- メーカー:FNA
- 包装:1set
- 価格:¥42,000
- 在庫:3個以上
- 納期:1週間程度 ※※ 表示されている納期は弊社に在庫がなく、取り寄せた場合の目安納期となります。
- 法規制等:
| 説明文 | タンパク質などの生体高分子を細胞内,特に細胞質に導入する試薬。タンパク質を細胞質に高効率に輸送することができるため,導入タンパク質の細胞内機能の評価や,抗体導入による機能阻害誘導など幅広い実験に使用できる。キット構成品 A:ProteoCarry 4 mg,B:FITC-dextran(positive control) 2 mg ※6ウェルフォーマットで14反応分相当。 |
||
|---|---|---|---|
| 法規制等 | |||
| 保存条件 | -20℃,暗所保存 | 法規備考 | |
| 掲載カタログ |
ニュース2023年6月15日号 p.29 ニュース2022年9月1日号 p.13 100周年ありがとうキャンペーン p.54
|
||
| 製品記事 | |||
| 関連記事 | プレインキュベーションが不要な新規タンパク質トランスフェクション試薬 ProteoCarry 販売開始のお知らせ トランスフェクション試薬選択ガイド トランスフェクション手法の紹介・比較 |
||

追加しました。
おすすめ製品記事
-
Nalge Nunc (サーモフィッシャーサイエンティフィック(株))
ART Pipette Tip(フィルターチップ/ノンフィルターチップ)
製品情報は掲載時点のものですが、価格表内の価格については随時最新のものに更新されます。お問い合わせいただくタイミングにより製品情報・価格などは変更されている場合があります。
表示価格に、消費税等は含まれていません。一部価格が予告なく変更される場合がありますので、あらかじめご了承下さい。