遺伝子発現に新たな選択肢。細胞の分化誘導に最適! センダイウイルスベクター作製受託サービス
掲載日情報:2023/06/01 現在Webページ番号:70990
(株)レプリテックでは、ご希望の遺伝子配列を搭載したセンダイウイルス(Sendai virus、SeV)ベクターを作製し、ご提供します。SeVベクターは幅広い細胞種への感染能力と、他のベクターに比べて高い遺伝子発現能力を有し、細胞のリプログラミングや分化誘導といった細胞改変で高い効果を発揮します。また、染色体に組み込まれないといった安全面の特長から、遺伝子ワクチン用のベクターや遺伝子治療用開発ツールとして注目されています。
追加しました。
- センダイウイルスとは
- (株)レプリテックのセンダイウイルス(SeV)ベクター
- 特長
- ウイルスベクターの比較
- SeVベクターとレンチウイルスベクターの遺伝子発現比較
- 関連受託サービス:温度感受性ウイルスベクター
- 受託サービスのフロー
- ご注文方法/価格
センダイウイルスとは
センダイウイルス
センダイウイルス(Sendai virus、SeV)は、一本鎖のマイナス鎖RNAゲノムを有するウイルスで、パラミクソ科に属します。SeVは細胞膜表面のシアル酸を認識、膜融合を引き起こすため、分裂・非分裂を問わず、血球細胞を含む幅広い細胞・組織に感染可能です。また、一本鎖のマイナス鎖RNAウイルスゲノムは細胞質に留まるため、宿主ゲノムには影響しません。さらに細胞質内でレプリコンを複製し、高い遺伝子発現が得られます。
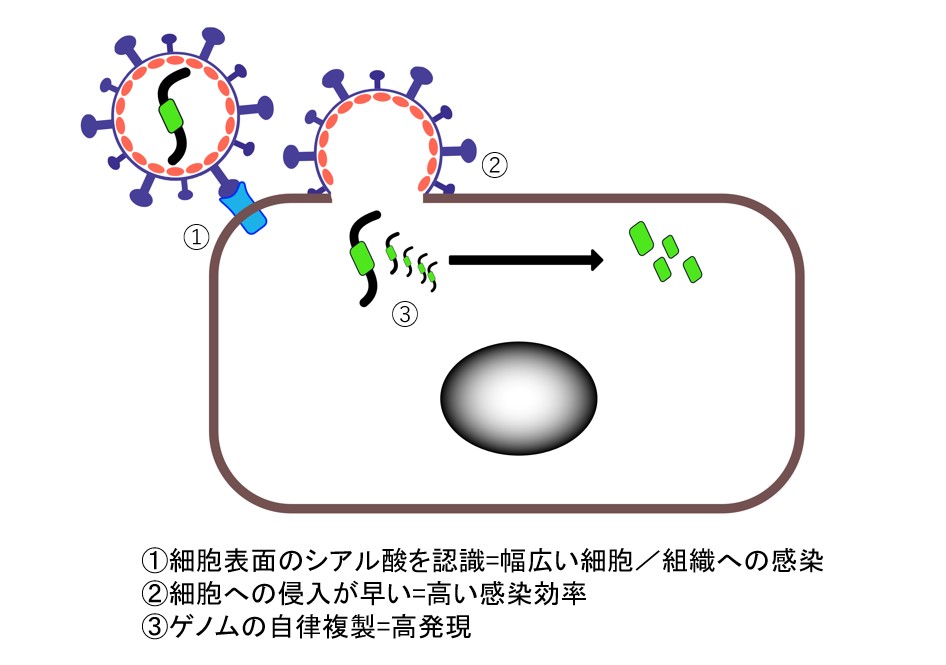
SeVの構造
SeVのRNAゲノムには3’端から順に以下のタンパク質がコードされています。
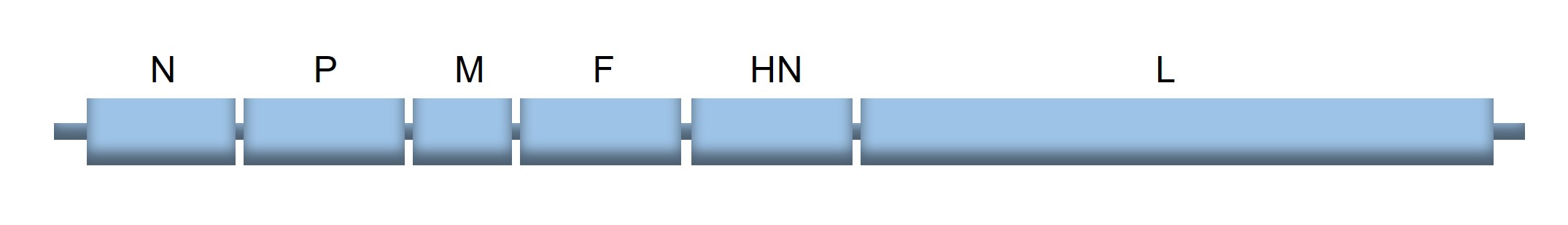
- N:RNAゲノムに結合するヌクレオカプシドタンパク質
- P*:RNAポリメラーゼの小サブユニットであるリン酸化タンパク質
- M:ウイルス粒子の膜構造を維持するマトリックスタンパク質
- F:細胞への侵入に関わる膜融合タンパク質
- HN:細胞との結合に重要なヘマグルチニン-ノイラミニダーゼタンパク質
- L:RNAポリメラーゼの大サブユニットであるラージタンパク質
* P遺伝子にはPタンパク質とは読み枠が異なるCタンパク質やVタンパク質もコードされています。
SeVの再構成と問題点
SeVベクターの調製には、SeVのRNAゲノムと構成タンパク質のN、P、Lが必須であり、ヘルパープラスミドや産生細胞からの供給が必要です。産生細胞内にこれらを遺伝子導入することでSeVが再構成されますが、SeVではこの再構成の効率が低く、十分な感染力価を得るためには時間を要することが知られます。また、SeVベクターを自家調製するためのツールが普及していないことが、SeVベクターがレンチウイルスベクター等、他のベクターのように広く利用されていない要因となっています。
参考文献
- 佐伯晃一『Medical Science Digest』, 48(13), 34~35(2022).
追加しました。
(株)レプリテックのセンダイウイルス(SeV)ベクター
(株)レプリテックではSeVベクターの再構成効率を劇的に向上させ、簡便にSeVベクターが得られるシステムの開発に成功しました。再構成効率は従来のセンダイウイルスベクター技術と比較すると1,000倍以上向上しています(下図1)。また、再構成開始3日目の培養上清を標的細胞に感染させた場合においても、従来技術をはるかに上回る高力価のベクター上清が得られています(下図2)。従来法の課題であった再構成効率を劇的に向上させることによって、手間と時間を短縮でき、これまで使用するのハードルが高かったセンダイウイルスベクターの提供が可能となりました。
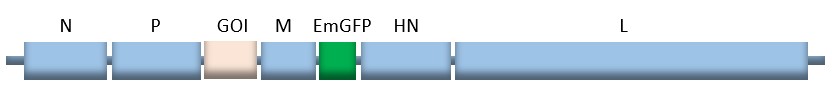
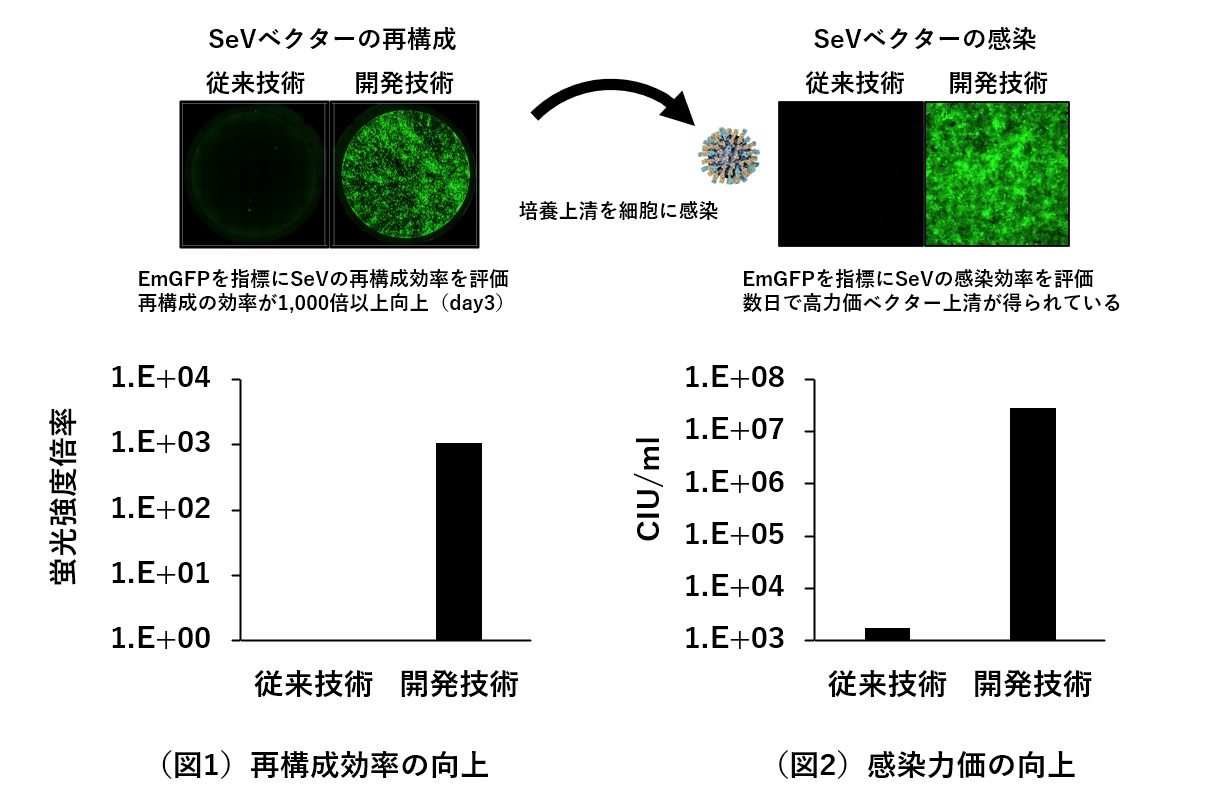
※ (株)レプリテックのセンダイウイルスベクターは、感染に必要なF遺伝子(Fusion Protein宿主の細胞膜とウイルスエンベロープを融合させる機能を持つ)を欠失させており、一度は感染できますが、その後の伝播性二次感染はありません。
追加しました。
特長
- 幅広い細胞・組織に感染可能
ほとんどの哺乳動物細胞膜上に存在するシアル酸を認識するため、分裂・非分裂を問わず多くの細胞種・組織に遺伝子導入可能(一部naÏve T細胞では導入効率が低い)。 - 高い感染効率
細胞への侵入が早く、短時間のウイルス暴露で十分な発現が可能。 - 高発現
導入細胞内でゲノムの自律複製が起き、高発現が期待できる。 - 低い遺伝毒性
ベクターゲノムは細胞質に留まり遺伝子発現するため、挿入変異や染色体の構造変化など宿主染色体に影響を与えない。 - 低い細胞毒性
宿主への細胞毒性が少なく、感染価に応じて発現量を調整可能。 - 安全性
センダイウイルス自体のヒトへの病原性が報告されていない。
追加しました。
ウイルスベクターの比較
| ベクターの種類 | センダイウイルス (SeV) | レンチウイルス | AAV | アデノウイルス |
|---|---|---|---|---|
| ゲノム構造 | 一本鎖RNA | 一本鎖RNA | 一本鎖DNA | 二本鎖DNA |
| 宿主染色体への挿入 | なし | あり | 低頻度 | 低頻度 |
| 発現 | 一過性発現 (2か月以上の発現も可能) | 安定発現 | 一過性発現 | 一過性発現 |
| 発現強度 | +++++ | +++ | ++ | ++++ |
| 導入効率 | +++++ | ++ | ++ | +++ |
| その他 | 染色体挿入無しに高発現 | 染色体への遺伝子挿入 | - | - |
参考文献
- Masaki, I., et al., FASEB J., 15(7), 1294~1296(2021).
- 小澤敬也『ウイルス』, 53(2), 163~170(2003).
- 飯田章博, 加藤篤『ウイルス』, 53(2), 171~175(2003).
- Oishi, K., et al., Cell Transplant., 18(5), 573~580(2009).
- 三宅弘一, 島田隆『日医大医会誌』, 8(2), 150~156(2012).
- Rao, M.S., et al., J. Cell Biochem., 113(10), 3061~3068(2012).
- Morimoto, S., et al., Genes Cells, 28(1), 29~41(2023).
追加しました。
SeVベクターとレンチウイルスベクターの遺伝子発現比較
各細胞にセンダイウイルス(MOI:10)およびレンチウイルス(MOI:10)を感染させ、3日後のEmGFPの蛍光を観察した。いずれの細胞においてもセンダイウイルスの方が遺伝子発現効率が高いことが示された。図の下の数値は、レンチウイルス感染に対するセンダイウイルス感染の蛍光輝度の倍率を示す。

追加しました。
関連受託サービス:温度感受性ウイルスベクター
(株)レプリテックでは温度感受性ベクターも提供しています。任意の遺伝子を発現させた後、導入したウイルスベクターを除去することが可能です。詳細はお問い合わせ下さい。
追加しました。
受託サービスのフロー
- お問い合わせ
発現させたい遺伝子、力価、必要量、プラスミド構築の有無など、詳細をヒアリングいたします。 - お見積り提示
ご提供いただいた情報を元に作製の可否などを検討し、お見積もりをご提示いたします。 - ご依頼
※ ご依頼の際には使用目的確約書をご提出いただきます。 - ウイルスベクター納品
目的遺伝子を組み込んだプラスミドベクターの構築、次いでウイルスベクターの作製を行い、作製したウイルスベクターをお送りいたします。
※ おおよその納期はプラスミド完成後1か月ですが、お客様のご依頼内容によって異なります。
追加しました。
ご注文方法/価格
詳細は当社受託・特注品担当までお問い合わせ下さい。
メーカーインタビュー:遺伝子発現に新たな選択肢

(株)レプリテックは、遺伝子ベクター技術や再生医療技術を有するバイオベンチャー企業です。
次世代型ウイルスベクターとしてセンダイウイルスベクターに着目し、従来の課題であった再構成効率を 1,000 倍以上改善させたベクターの開発に成功しました。
追加しました。
製品情報は掲載時点のものですが、価格表内の価格については随時最新のものに更新されます。お問い合わせいただくタイミングにより製品情報・価格などは変更されている場合があります。
表示価格に、消費税等は含まれていません。一部価格が予告なく変更される場合がありますので、あらかじめご了承下さい。

