HOME > 受託サービス・特注品 > 創薬・薬物動態 > 安全性試験 > 薬剤感受性試験受託サービス
高精度表面プラズモン共鳴法(HP-SPR法)による薬剤感受性試験 薬剤感受性試験受託サービス
掲載日情報:2017/07/25 現在Webページ番号:65675
新開発の高精度表面プラズモン共鳴法(HP-SPR法)を用い、生理的濃度での生理活性物質(候補)の薬効および毒性評価を同時に行うスクリーニングサービスです。従来の細胞の共培養法は、薬効や毒性評価に少なくとも7日間を要しましたが、レーザー照射によるミトコンドリアの分極変化率と細胞の最終挙動との定量的な相関性に基づくHP-SPR法は、薬物投与約1時間で結果が得られます。ご要望により、ヒト消化・吸収モデルを用いて試料を処理した後、同試験を行います(オプションサービスで別途料金が掛かります)。
追加しました。
- 薬剤感受性試験(HP-SPR法)の種類と適用
- 薬剤感受性試験における共培養法と高精度プラズモン共鳴法(HP-SPR法)-3Dとの比較
- 高精度表面プラズモン共鳴法(HP-SPR法)とは
- 薬剤感受性試験(HP-SPR法)の実施例 1
- 薬剤感受性試験(HP-SPR法)の実施例 2
- ご注文方法/価格
薬剤感受性試験(HP-SPR法)の種類と適用
生体内と同様のin vivo -likeスクリーニングを、各種生細胞を用い、抗がん物質のような薬物(候補)や生理活性成分に対して行なう受託試験サービスです。対象試料を送付して頂き、必要に応じてヒト消化・吸収モデルを用いて試料を処理し、薬効を示す濃度範囲、およびアポトーシス(細胞は自殺するが他の細胞には影響を与えない:言わばイエローゾ-ン)、並びにネクローシス(細胞が爆発して他の細胞に炎症などの影響を与える:言わばレッドゾーン)毒性を示す濃度範囲をデータとしてフィードバックします。
| 確立しているアプリケーション | 適用可能なアプリケーション*1 |
|---|---|
| 1. 抗がんスクリーニング | 1. 抗アルツハイマー |
| 2. 脂肪燃焼促進 | 2. 抗糖尿病 |
| 3. 代謝活性化 | 3. 抗てんかん |
| 4. アンチエイジング | 4. 育毛促進 |
| 5. 肌のターンオーバー促進 | 5. 美白促進 |
| 6. 冷え性改善 | 6. 肌のしわ予防 |
| - | 7. 免役活性化 |
| - | 8. 骨形成促進 |
| - | 9. 各種細胞毒性 |
*1 研究期間を要するために、評価結果が出るまである程度の期間を要します。詳細については、当社特注品・受託担当までお問い合わせ下さい。
追加しました。
薬剤感受性試験における共培養法と高精度プラズモン共鳴法(HP-SPR法)-3Dとの比較
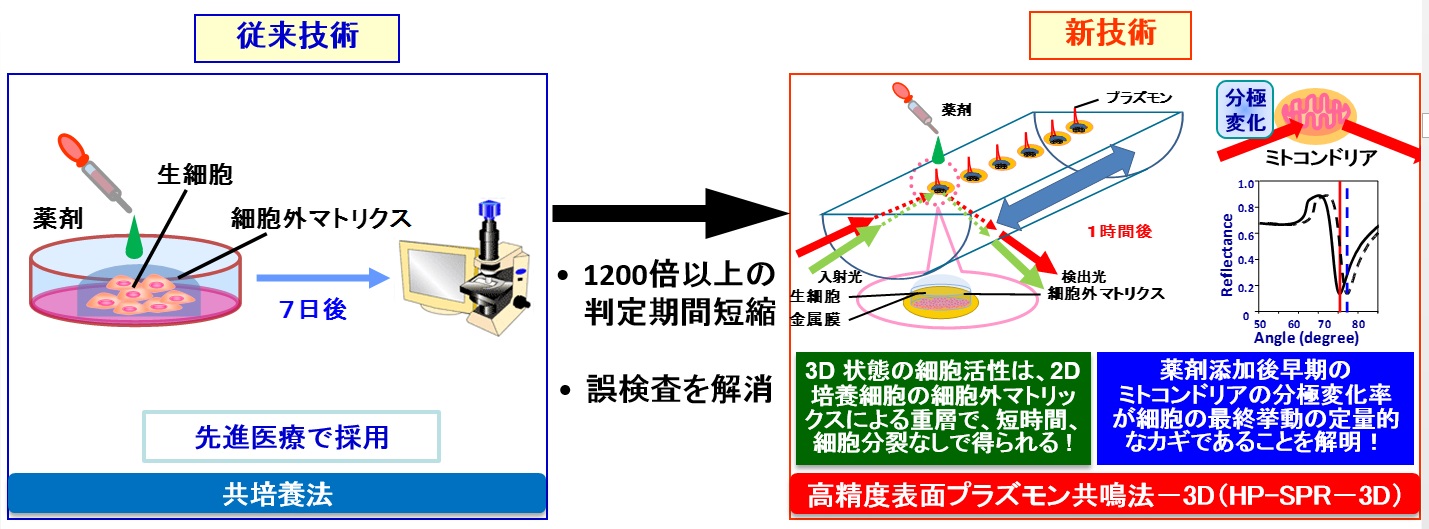
※ 画像をクリックすると拡大図をご覧いただけます。
| アッセイ法 | 共培養法(セルベースアッセイ) | HP-SPR-3D法 |
|---|---|---|
| 細胞と環境 | 細胞外マトリクスと三次元培養 | 二次元培養細胞を細胞外マトリクスで被覆 |
| 細胞状態 | 生体内の細胞状態を培養により再現 | 培養せず短時間で生体内細胞状態 |
| 培地交換 | 定期的に必要 | 不要 |
| 判定期間 | 長い培養・判定期間(7~30日)⇒遅 | 迅速判定(1時間以内の10分間程度)⇒速 |
| 臨床との関係 | 標準法⇒高信頼 | 生体内レベル標準法結果と互換⇒高信頼 |
| 適用薬剤・個人 | 薬剤の作用機構・個人差関係無⇒高信頼 | 薬剤の作用機構・個人差関係無⇒高信頼 |
| 判定誤差 | 蛍光判定試薬必要⇒誤判定⇒低信頼 | 光で直接検出⇒試薬不要⇒誤判定無⇒高信頼 |
| 効果・毒性同時判定 | 難⇒低信頼 | 易⇒高信頼 |
| 手技 | 煩雑⇒労力大+多検体処理難⇒遅 | 簡便⇒労力小+多検体処理可⇒速 |
| 必要細胞数 | 多(~106個) | 極少(1,000個) |
| 価 格 | 高 | 安(1/8程度) |
追加しました。
高精度表面プラズモン共鳴法(HP-SPR法)とは
高精度表面プラズモン共鳴法(HP-SPR法)は、レーザー分光法の一種で、HP-SPRセンサーを用いて非標識、リアルタイムで分子間相互作用などに由来する検出領域の屈折率変化を検出する装置および技術です。HP-SPR法は、世界で初めて生細胞の応答の定量化を実現した、画期的な薬剤効果の評価方法です。HP-SPR法を用いることにより、ミトコンドリアの分極状態を非標識、非侵襲的に高感度、低エネルギースキャンでリアルタイムモニターが可能です。ドラッグデリバリーにおける効果の確認にも対応しています。さらに、HP-SPR法では細胞培養が不要なため、iPS細胞などの健全な長期細胞培養が困難な病態モデル幹細胞の利用による新薬開発に特に有効です。
HP-SPRセンサーでは、生細胞内のミトコンドリア内膜の誘電率に基づく電位差(分極)の検出が可能です。
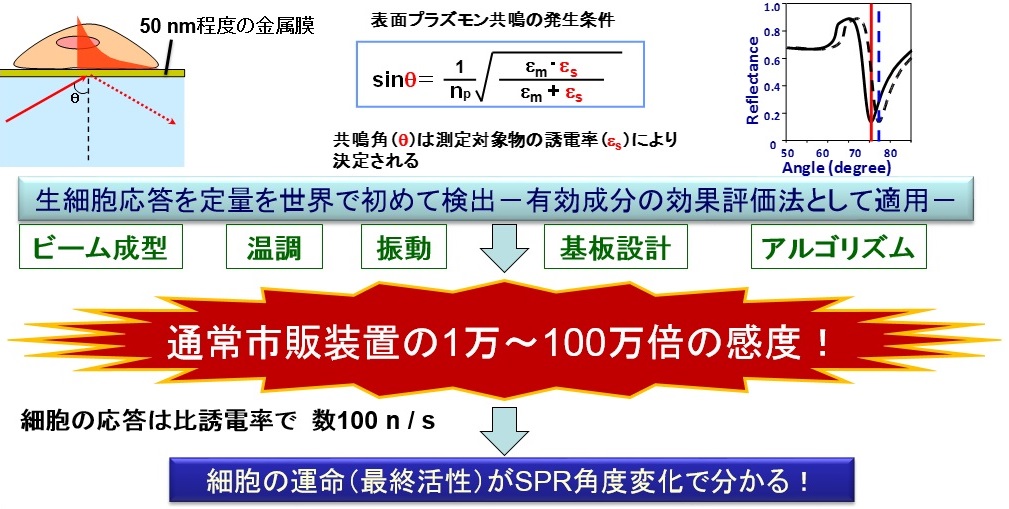
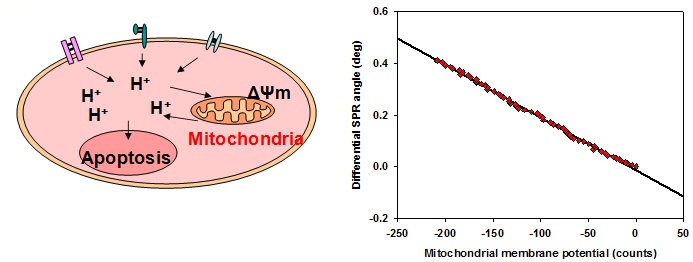
左:ミトコンドリア内膜における分極
右:SPRアングルとミトコンドリア膜電位(特異的インヒビターを用いた蛍光を検出)による測定結果
上部に落射型蛍光顕微鏡、下部にSPRを配置した装置により、SPR基板上にヒトすい臓がん細胞MIA PaCa-2を自己接着させた後、ミトコンドリア膜電位感受性蛍光色素(JC-1 iodide)を導入し、CCCP(Carbonyl cyanide m-chlorophenylhydrazone)によりミトコンドリア膜電位変化のみを誘導した。蛍光とSPRを同時観察すると、膜電位変化に応じてSPR シグナルの変化が観察された(P<0.001)。
追加しました。
薬剤感受性試験(HP-SPR法)の実施例 1
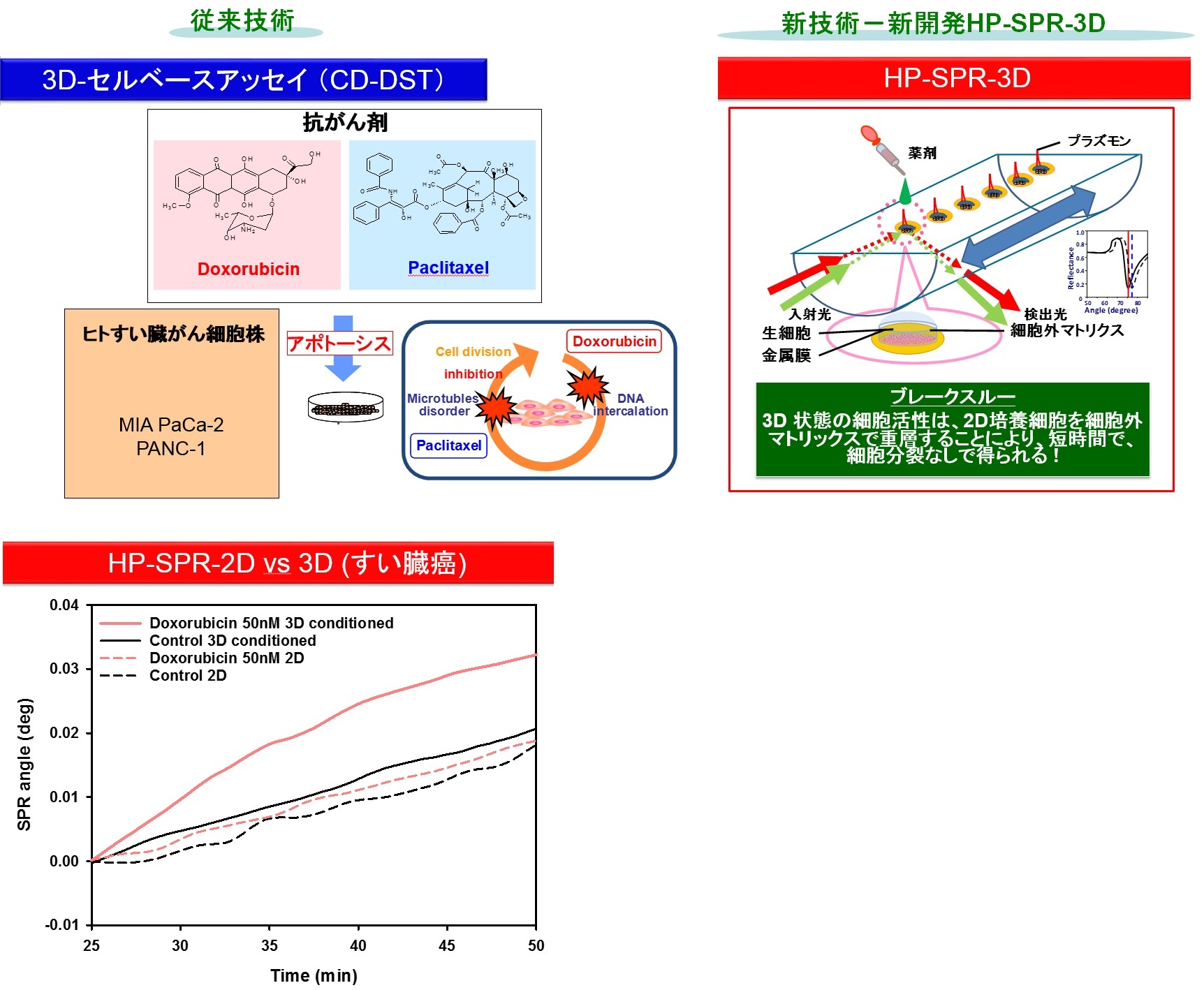
(1)HP-SPR(-3D)を用いたすい臓がん細胞の活性化測定(図2)
詳細は、こちらをご覧下さい。PDFファイルがダウンロードできます。
(2)HP-SPR(-3D)を用いたすい臓がん細胞への細胞毒性評価試験(図3)
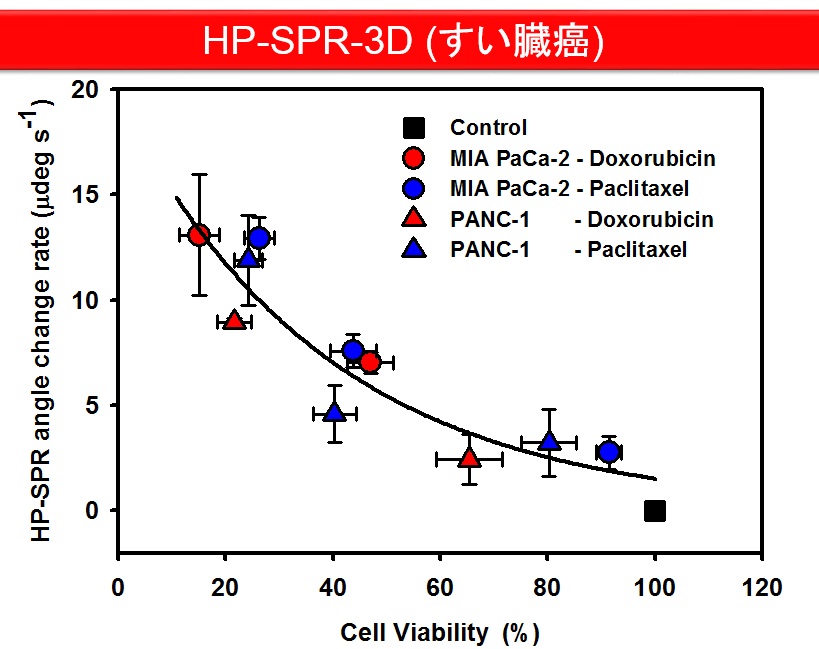
詳細は、こちらをご覧下さい。PDFファイルがダウンロードできます。
(3)HP-SPR(-3D)を用いた冷え性改善評価試験(図4)
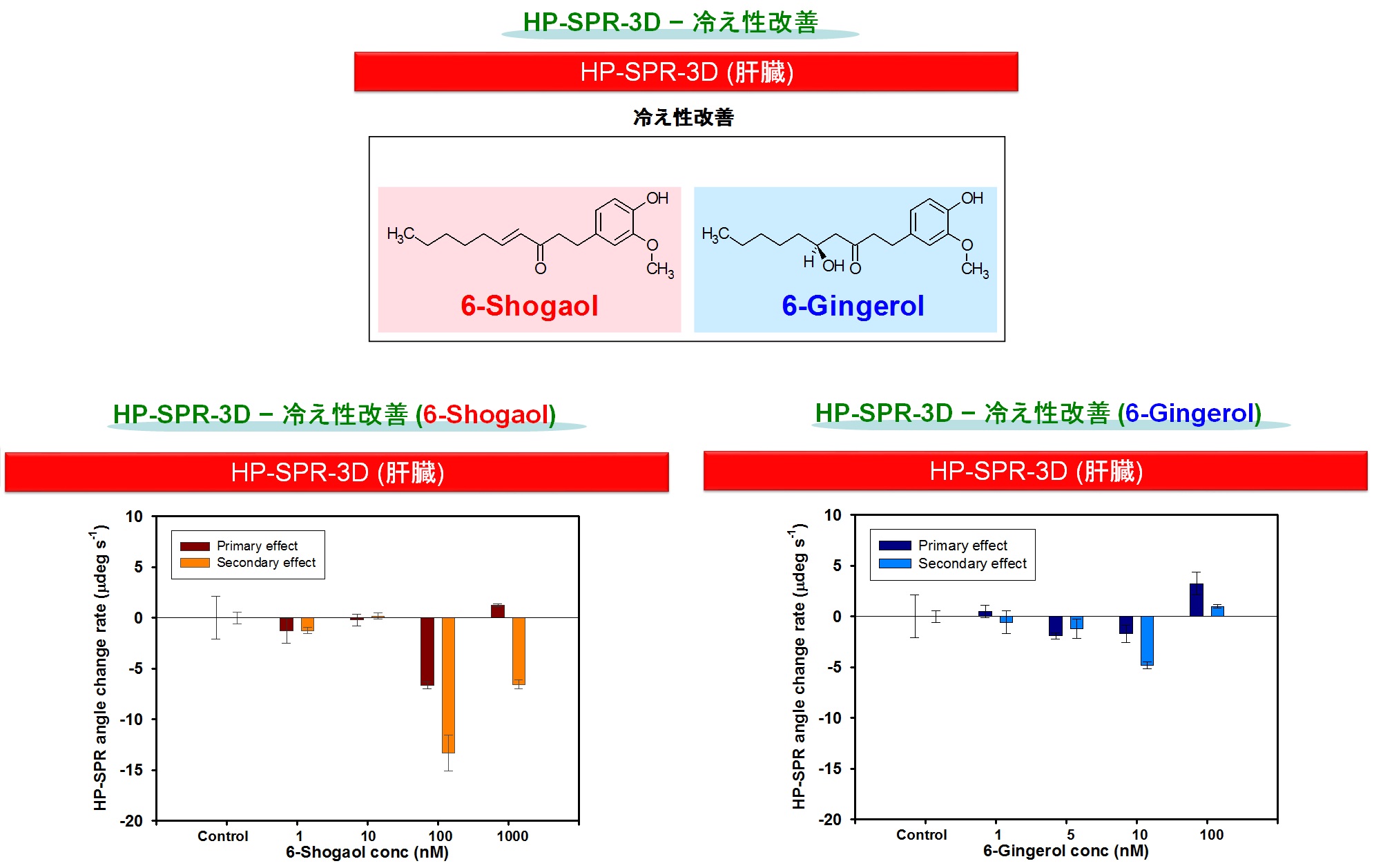
詳細は、こちらをご覧下さい。PDFファイルがダウンロードできます。
(4)HP-SPR(-3D)を用いた肌ターンオーバー促進効果の評価(図5)

詳細は、こちらをご覧下さい。PDFファイルがダウンロードできます。
■参考文献
- Ona, T., et al., ALTEX Proc., 3, 24 (2014).
- Ona, T., et al., FRAGRANCE J., 42, 50 (2014).
- Ona, T., et al., J. Pharm. Sci., 121, 132 (2013).
- Ona, T. et al., J. Pharm. Sci., 121,159 (2013).
- Nishijima, H., et al., Anal. Sci., 26, 529 (2010).
- Ona, T. et al., Anal. Bioanal. Chem., 398, 2505 (2010).
- Kosaihira, A., et al., Anal. Bioanal. Chem., 391, 1889 (2008).
- Ona, T., et al., Biophotonics, 9, 69910R (2008).
追加しました。
薬剤感受性試験(HP-SPR法)の実施例 2
【目的】国内産の巨峰からタネを取り出し、これを休眠打破することにより内容成分の相転移を促し、ブドウ種子エキスの膵がんに対する薬効・毒性の評価を行った。この際、経口投与を想定し、ヒトモデル系による消化・吸収処理した後供試した。方法として、三次元(3D)細胞培養のようなin vivo-like薬剤感受性試験である、独自の新規1hフェノタイピック・スクリーニング法、高精度表面プラズモン共鳴法(HP-SPR-3D)を用いた(図1)。
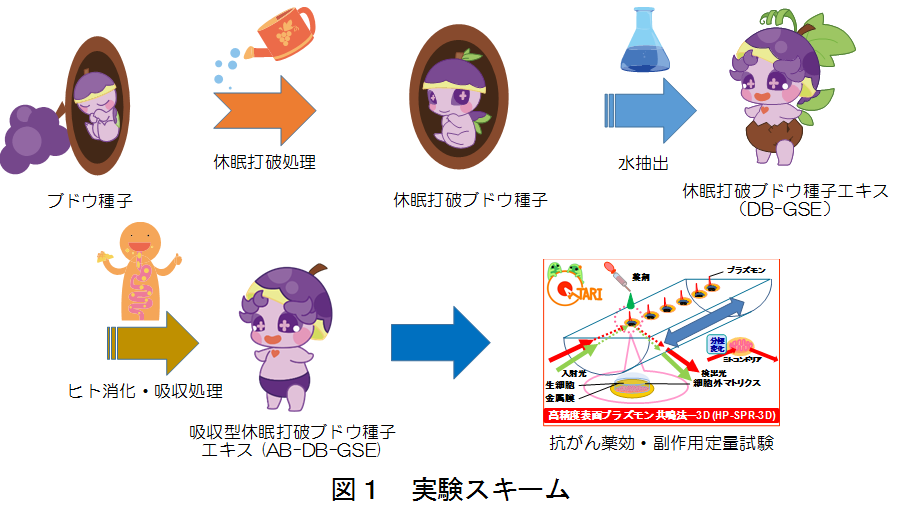
【実験】供試資材として、福岡県久留米市田主丸産の巨峰ブドウのタネを休眠打破、粉砕、抽出および乾燥した後用いた。ヒトモデル系を用い、胃ステップおよび十二指腸ステップでの消化後、分子量10,000以下を腸管吸収成分として次の薬剤感受性試験に用いた(図1)。市販抗がん剤としてドキソルビシン、パクリタキセルおよびゲムシタビンを用いた。供試細胞としてヒト膵がん細胞株Mia PaCa-2を用いた。二次元培養した生細胞をHP-SPR-3Dセンサーチップ上に自己接着させた後コラーゲンを重層し、試料を投与後1時間の細胞応答の経時変化を測定した。HP-SPR角度の経時変化と、臨床と相関がある3D細胞培養法であるCD-DST法による細胞生存率との検量線を用いて細胞生存率を計算した。
【結果】薬効は濃度依存性があり、2.5 mg/ml以上で効果が認められ5.0 mg/mlで最大であった。これ以上の濃度では細胞の機能停止と考えられる毒性を示し、一般的なネクローシスとは異なっていた。なお、2.5 mg/mlより低い濃度では、胆汁の影響から膵がん細胞が活性化され負の効果が認められた(図2)。細胞生存率では、静脈内投与で用いられる市販抗がん剤であるドキソルビシン、パクリタキセルならびにゲムシタビンと同等、またはこれら以上の膵がんに対する薬効が得られた(図3)。特筆すべきは、今回の休眠打破ブドウ種子エキスでは、経口投与を想定したにもかかわらず高い効果が見られた点である。
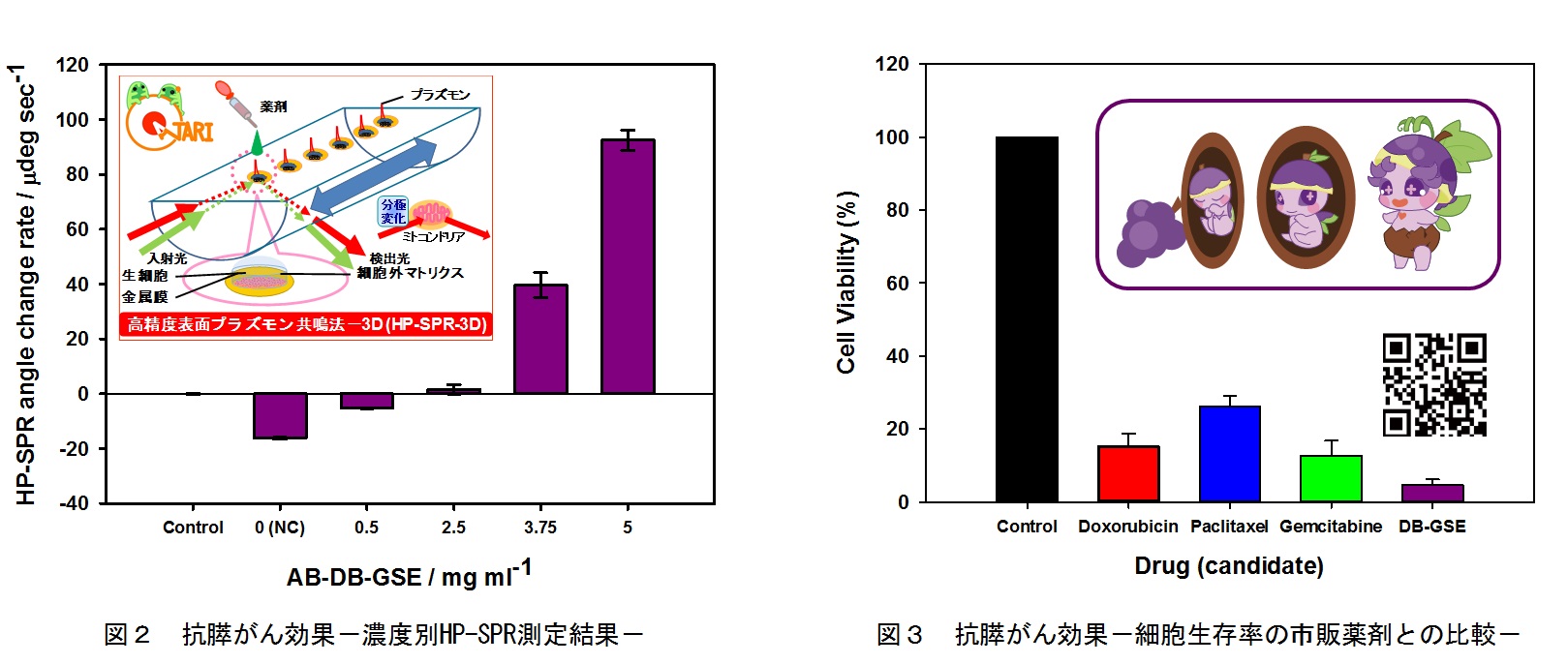
追加しました。
ご注文方法/価格
価格、納期はその都度お見積りします。詳細は当社受託・特注品業務担当までお問合せ下さい。
追加しました。
製品情報は掲載時点のものですが、価格表内の価格については随時最新のものに更新されます。お問い合わせいただくタイミングにより製品情報・価格などは変更されている場合があります。
表示価格に、消費税等は含まれていません。一部価格が予告なく変更される場合がありますので、あらかじめご了承下さい。


